そいつは牛だ!!って言われそうですが、
生きている牛は死んでいる人に勝ります。
生きたまま裂く訳じゃないんですけど・・・
■セシウムは、内部被曝の枠をとりあえず外れます。
内部被曝よりもセシウムの毒性が上回るから。
■そのほかのストロンチウムとか一応、放射線管理となると思います。
水のトリチウムはとりあえず無視します。
バックグラウンド的には人の成分の7割は水なので
50キロの人で35キロの水分があり、100ベクレルオーダーだと
よろしくないですが、
まずは、そんなにはなっていないと思いますので
「取らないに越した事はない」という判断です。
セシウムをもう一度考えましょう。
■まず、血液の汚染が最初にあって(30ベクレルが一つの区切り)
比較的その濃度に追随する筋肉(20倍、相関くっきり)
噂されていた心臓(10倍、相関ぼんやり)
沈黙の排出系臓器肝臓(10倍弱)
■要は血中管理です
カリウムの吸収過程がその参考になるでしょう。
速やかに血中濃度が上昇し、排泄と摂取が起きて、
バランスを取っているという事になります。
腸管におけるKイオンの吸収分泌の細胞機序とその調節機序
本研究の目的は、腸管におけるK輸送の細胞機序やその膜輸送分子実体をさらに明らかにするとともに、その輸送活性調節機序を明らかにすることである。
まず、ヒトにおけるカリウム投与後の血清中及び尿中の電解質変化を検討した。
その結果、カリウムを投与すると速やかに血清中のカリウム濃度が上昇し、尿中へのカリウム、ナトリウムおよび塩化物イオン排泄が同時に亢進されることが明らかになった。「予測制御」の存在は肯定されなかった。次に、ラット腸管K吸収に関し、非吸収性マーカーのポリエチレングリコールを用い検討した。
その結果、摂取したKの大部分は小腸上部で吸収iされた。吸収は主として濃度勾配の依存しており、小腸に顕著なK吸収調節機序があるようには見えなかった。次に、マウス回腸におけるK輸送をUssing chamberを用い検討した。吸収方向のKフラックスは分泌方向のカリウムフラックスより大きく、能動輸送による吸収機序の存在が示唆された。さらに、マウス遠位大腸のK輸送もUssing chamber法で検討した。ouabain感受性のK吸収機序と、管腔側TEAと漿膜側bumetanideで抑制されるK分泌機序が存在することが示された。β受容体刺激薬や高K食でK分泌は増大することが示された。次に、モルモット遠位大腸管腔側膜H^+,K^+-ATPase,漿膜側Na^+,K^+-ATPaseのOuabain用物質に対する感受性の比較を行ったところ、ouabainは両者を同程度の抑制した。その他の物質は何れもH^+,K^+-ATPase活性をNa^+,K^+-ATPase活性より、より低濃度で抑制した。最後に、ラット遠位大腸をUssing chamberに装着し、aldosteroneを投与したところ、K分泌を表すTEA感受性の短絡電流は4時間後から有意に増大し、Na吸収を表すBenzamil感受性の短絡電流も4時間後から増大した。
ウィキ2連発
■K(カリウム)の人体内のふるまい [編集]維持輸液で必要なカリウムは一日あたり20~40mEqであるが、経口摂取では一日50~100mEq必要であるといわれている。正常人ではKは摂取量と同じだけ尿中に排出されることが知られている。即ち、腎障害がなければ尿中カリウム量からカリウム摂取量を予測することができる。
■カリウムの吸収は40%なので、セシウムも40%と見たほうがいいでしょう。
ただしホメオスタシスの都合上、また濃度勾配に依存しますので、
血中濃度が低下していれば、より吸収率は上がり
血中濃度が上がっていれば、吸収率はやや、下がる方向に行く
(尿による排出でバランスを取るようですね。)
部分排泄率(fractinal excretion;FE)とは腎臓学で使われる指標のひとつであり、ある電解質のクリアランスをクレアチニンクリアランスで割ったものである。腎不全で脱水によるものか、腎障害によるものかを判別するのに用いるナトリウム部分排泄率が有名である。
血清レベルの変化と部分排泄率の変化の組み合わせで血清レベルの変化が腎からの排出変化が主体であるのか否かを判断することができる。
血清レベルが上昇しているとき
部分排泄率増加→過剰摂取
部分排泄率低下→腎からの排出低下
血清レベルが低下しているとき
部分排泄率増加→腎からの排出亢進
部分排泄率低下→摂取不足
これは摂取量が多ければ、尿中の排泄量は増加し、少なければ低下するというホメオスタシスの考え方と一致する。
有名な部分排泄率 [編集]ナトリウム部分排泄率
これが1%未満であったら脱水を考える。腎前性腎不全の所見である。
カリウム部分排泄率
正常は12.5~25%である。カリウムは摂取量と排出量が等しくなる数少ないイオンである。
■臓器の健全性がある場合、
良質のカリウムを体内に供給するのは有効な手段といえるだろう。
腎臓機能に負担をかけると悪い結果が起きるともいえる。
逆に言えば血液レベルで、カリウムは抑えられている
一度体内に入れば、尿中か、体内取込かのどちらかが起きる。
変な物がなるべく入ってない水(カリウム含有)を多く飲むのが、
もっとも理想的、となる。
気になるインシュリン(糖代謝に関わる)
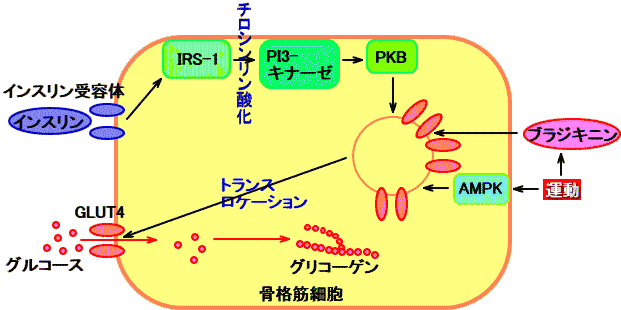
■2.インスリンは、GLUT4を介する細胞内へのグルコース取り込みを、促進させる
膵臓のラ氏島β細胞は、組織中のブドウ糖濃度に反応し、インスリンを分泌する。
インスリンが、筋肉細胞や脂肪細胞に存在する、インスリン受容体に結合すると、チロシンキナーゼが活性化されて、IRS-1(insulin receptor substrate-1)などがチロシンリン酸化される。
IRS-1のリン酸化チロシンに、PI3-キナーゼ(phosphoinositide 3-kinase)、Grb2・Sos複合体、SHP-2が結合する。
PI3-キナーゼが活性化され、プロテインキナーゼB(PKB、Aktとも呼ばれる)が結合する。
PKBは、PDK1(phosphatidylinositol-dependent protein kinase 1)によりリン酸化され、活性型PKBになる。
活性化PKBは、細胞膜を離れ、種々の蛋白質をリン酸化する。
そのため、筋肉細胞(骨格筋、心筋)、脂肪細胞では、糖輸送担体(グルコーストランスポーター:glucose transporter)のGLUT4(グルットフォー:glucose transporter 4)含有小胞の細胞膜への移動(トランスロケーション:translocation)が促進され、細胞膜上にGLUT4が発現され、細胞内へのグルコース(ブドウ糖)の取り込みが促進される。
この時、K+も、細胞内に取り込まれる。
このように、GLUT4は、インスリン反応性組織(筋肉細胞、脂肪細胞)に発現し、インスリンに反応して、グルコース(ブドウ糖)とK+を、細胞内へ取り込む。
活性化PKB(Akt)は、インスリンの蛋白質合成の促進作用、グリコーゲン合成酵素の活性化作用にも関与している。
肝細胞では、グリコーゲン合成酵素が活性化され、グルコースからグリコーゲンが合成される。
取り込まれたグルコースは、グリコーゲンとして筋肉や肝臓に貯蔵ざれたり、解糖系を経て中性脂肪として脂肪組織に貯蔵される。
インスリン受容体の数は、インスリン濃度が増加すると減少する(down regulation)。
たぶん山さんの脂肪細胞はこれを言っているのかなと、
でも脂肪周りのセシウムは・・・害なさそう、死んでもいいや。
排出は遅れますが特濃じゃないとき害あるかな・・・
霜降りだとあるか(苦笑)
■カリウムイオンの取り込みはこのように濃度勾配による吸収
糖代謝の経路に沿って集中していくと思われます。
セシウムはここまでは一緒ですが、ここから濃縮が始まると思われます
(カリウムチャネルに15%でなかなか侵入できない)
■ここからはセシウムの電気的機序につながります。
2011年11月16日
東北大モデル(牛)のポイント。と内向きカリウムチャネルの重要性
結果的に溜まったセシウムイオンは何かを邪魔していくという
 東北大の牛の推察から食の取り方を考えるための勉強
東北大の牛の推察から食の取り方を考えるための勉強

 今、あなたにおすすめ
今、あなたにおすすめ