2012年01月10日
【今更紹介?】放影研のラジカル紹介が分かりやすい【・・・こんな書いていいの?】
の続き的なエントリーです。
■今回はちょっと「人格を変えて」お送りします。
猛走峠さん辺りなら意味が分かるかも?
■やい、低線量被曝基地害ども!!
良く耳をかっぽじって見やがれ!!
訳の分からないプロパガンダ流すなら、
とっとと危ない国から出てけ!!!
DNAはベイスターズだけで十分で
被曝の本筋はラジカルだって
村人がちゃんと議論してるんだよ!!
***********************
早くも疲れました^^;突込みどころをもうけて終わった。
■
村人はきちんと、討議してる。
正体はラジカルだってことも知ってる。
DNAヒットしなくても
細胞質ヒットでまずいことも知ってる。
うん、細胞質に意味があるらしいんだわ。
アルファ線とかもあんまり関係ないらしい・・・

全体として変わらないらしいから・・・
厄介なのは死ぬべき人間が死なずに
死なないべき人間が死ぬことだ
↓
極めて統計の影響が出にくい
集団での死者はあんまり変わらない。
*************************
■そう、全体の死者はあまり変わらない。
影響がないわけじゃなくて、
特に低線量被曝の場合・・・
放射線で人が死ぬ分、放射線で人が生きる。
だから往々にして放射能で
人が死ぬと叫んで95才とかの人がいる。
叫んでいる本人は長生きの恩恵を生かして
ごねている可能性がある。
と、言うわけで
目からうろこの談義が続きます。
***********************
■
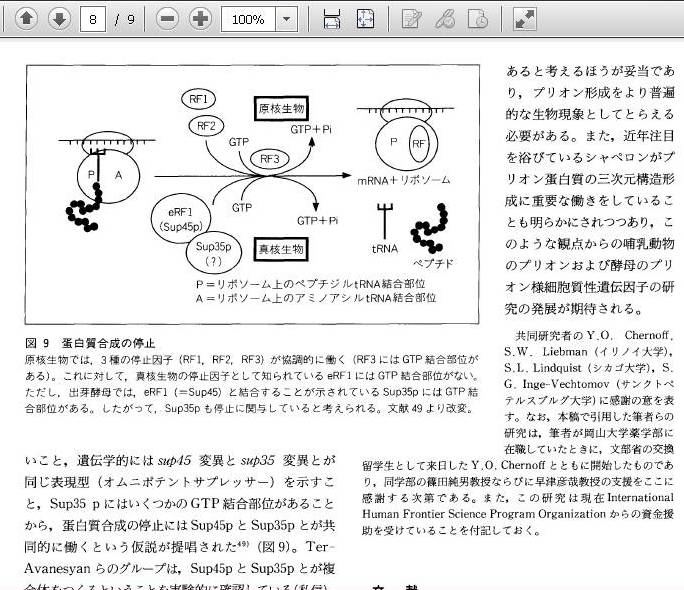
何より面白いのはBystander効果。
細胞質に含まれる酵素なのか、
あるいはリボゾーム蛋白なのか?
そういう転写系の物のエラーの方が
よほど遺伝子異常を起こしやすいと言う話。
そりゃ、教科書や原典書き換えるのは無理でも
手作業で写本すれば間違えるわけで・・・
詰り放射線の害なんて物はまやかしであると言うこと。
おまけのラジカルこそが注目だよと言うことは
村人はとっくに知っていて、
なぜか黙っている。
で、反原発&放射線「基地外」達が
デマや、間違った情報や、誤解や曲解を持って
ギャースカギャースカ叫んでいる。
人間はそんなヤワじゃない。
但し、放射能感受性が高いか低いか
また放射線がいい方向に働くか、
悪い方向に働くか?
そこの悪魔的くじ引き券を、
日本国民が何枚かずつ渡されているだけです。
福島県民は見ないことをお勧めする・・・
突込みどころが満載なのです・・・
リンパ球のライフタイムが短くなって、
ターンオーバーが変わるとかさ・・・
細胞質に照射するだけで
染色体異常は沸くんだよとか
がんは最後だから、とか。
人の体ってすごい。
放射線=薬の人もいる。
放射線=毒の人もいる。
残念ながら、避難することで
死ぬ人も確実にいると言うこと。
**************************
第8回 低線量放射線影響分科会速記録
原子力安全委員会
(注:
この速記録の発言内容については、発言者のチェックを受けたものではありません)
第8回低線量放射線影響分科会議事次第
1.日 時 : 平成14年5月16日(木)10:00~12:00
2.場 所 : 原子力安全委員会第1、第2会議室
引用①
>○佐々木委員 私は、この報告書は、まず発がんに絞るということだから、染色体をやるとまたややこしくなると思うんですよね。ただ、私は、ここでこれが文章が出てきたとすると、文章があると非常にミスリーディングに、染色体異常が出なきゃ発がんはないのかというような、そんなことを考えている人は誰もいないのであって、だから、これを取れば非常に明確になるんじゃないかと思うんです。
ただ、
島田委員もおっしゃったように、例えば、なお、リンパ球の不安定型染色体は被ばく線量に対応して上昇していることが確認されている。ということは、その中で統計的に有意に発がんが上がってないということが非常に意味があるということだと思うんです、フィジカルドジメトリーの補完という意味で。それが一つと、僕が言うとぶち壊しになるから……。
○丹羽主査 それじゃ、とりあえずですけれども、不安定型のやつが増えるというデスクリプションをここに入れて、今の安定型以降のやつを取り去るということでよろしゅうございますか。
引用②
>
○渡辺委員 だから、がんに結びつくかどうかというのは、今の段階でもオーバーエストメーションでしょうけど。
○丹羽主査 そうじゃなくて、佐々木先生がおっしゃるのは、2つ可能性があって、ハイバックグラウンドの中にもぐっているから見えないという考え方と、マヤックのデータを見ても、やはり安定型は増えてないというか不安定型が突出するということなんで、別のでもあるかもしれない。その両方でということですよね。
○佐々木委員 ええ、そうです。だから、低線量率をやって上がらないという人も、今の段階では、どの著者も、要するにメカニカルに上がらないんだとか、生物学的には上がらないんだとか線量率問題であるとか言わないで、どれもフィジカルドースエスティメイトがオーバーエスティメイトじゃないかというディスカッションです。
私は要するに、上がらないのは、やはり低線量率の問題は単純にDDREFで片づけられない、もっと生物学的な問題があると私は個人的に思っているんですよ。だけれども、それは個人的に思っているだけであって、例えばこの間の菅原先生のシンポジウムなんかでは、要するに、そういうやつをやったシンクレアも全然問題にもそんなのないよといって、今、アメリカでは線量のドジメイトを再評価しているんだということです。
それから、中国のハイバックグラウンドが不安定型が線量に比例して上がるというのは、あれはえいやと引けば直線ですけれども、あれはきちっとリンパ球の寿命を考慮してできたやつは寿命とともになくなっていくとやると、あのやつはもうちょっと上がるんです、こういうふうに。ただ、普通のあれは、子供のときからずっと浴び続けてますから、リンパ球のライフタイム自身が年齢とともに変わるんです。だから、一応4分の3ルールというのを適用して、だから、20歳ぐらいまででアダルトのライフタイムになって、それまでは年齢の逆にしてリンパ球のターンオーバーが早いとして、それで計算すると、大体ああいうふうになるんですよ。だけれども、直線ではないんですけどね。
だから、あれはそういうリンパ球の寿命で、捨てられる部分も考慮してないと、ただえいやと線を引いているから直線、あるいはメカニカルにプロポーショナルだと理解するのはおかしいと思うんです。
○島田委員 僕の今までの理解が間違えているのかもしれないんですけれども、染色体異常と発がんとの因果関係ではなくてコリレーションの疫学データというのは今までは、例えば、ここは佐藤先生は安定染色体異常のことを書かれてますけれども、
例えば不安定染色体異常でも、中国のほかの地域では安定染色体異常の報告もあったと思いますけれども、染色体異常が増えているけれども、つまり、それぐらい被ばくをしているけれども、がんはその地区では上がっていませんでしたというふうな解釈の論文が多いんじゃないかなと思うんです。つまり、染色体異常が不安定型でも安定型でも上がって、確かに被ばくはしている。でも、その地区ではコントロール群と比べてがんの率は上がっていませんでしたよというのが今までのこういう染色体異常と発がんとのコリレーションの論文の多くのストーリーじゃなかったかなという気はしていたんですけれども、違いますか。
○佐々木委員 だから、そういうふうに記載するのが正しいと思うんです。だから、線量評価の問題をそれである程度クリアできるんですよね。
引用③
>○酒井委員 まず、変換ミスを訂正をお願いいたします。
499行目「染料率」、失礼いたしました。
読ませていただきます。
放射線適応応答の研究の現状
放射線適応応答は、低線量放射線を予め照射しておくことによりその後の高線量放射線に対する抵抗性が誘導される現象を指す。 最初の報告はヒト末梢血リンパ球における染色体異常を指標としたものであった(Olivieri et al .1984)その後、種々の培養細胞において、染色体異常、小核形成、姉妹染色分体交換、突然変異誘発、悪性形質転換などを指標として適応応答が報告されている。ただし、指標によってはその有無について結果の一致が見られないものもある(参考資料1、Sasaki 1995、Wojcik and Shadley2000)。
また、個体レベルにおいてもマウスの骨髄死を指標とした報告がある(委員参考意見1)。
典型的な実験手法としては、先ず低線量の照射を行い、その後時間間隔をおいてから高線量の照射を行った後に種々の指標の解析を行うという段取りになる。その観察のために高線量を必要とするので、放射線防護基準で考慮するような低線量放射線のリスク評価には影響を与えないとされることもあるが、高線量照射は低線量事前照射によって誘導された「抵抗性」を顕在化させるための手段ととらえるべきである。
これまでに明らかとなってきた適応応答の一般的な特徴として、(1)放射線抵抗性の獲得までに時間を要し、この間に遺伝子の新規発現誘導が必要であること、(2)比較的限られた線量範囲(数十ミリグレイから数百ミリグレイ)の事前照射のみが有効であること、(3)獲得された抵抗性は一時的なものであること、(4)遺伝的背景に依存することなどが挙げられる。
2.放射線防護体系に反映させるまでに考慮すべき(情報を集めるべき)問題点
適応応答は、放射線障害を軽減する方向に作用する生体の応答のひとつであることは間違いないが、放射線防護において問題となる長期にわたる発がんリスクの低減につながるかどうかは検討を要する。また、これまでに得られている情報の大部分は高い線量率で短時間の内に事前照射を行ったものであり、この現象を放射線防護体系に反映させるためには、(1)個体レベルにおける発がんに関する適応応答の有無、(2)低線量率長期照射の場合に適応応答誘導の線量・線量率依存性とその持続性、および(3)適応応答に関与する遺伝的背景に関する情報が必要であり、これらの問題に取り組んだ報告を重点的に収集すべきであろう。高バックグラウンド地域の住民の健康調査あるいは「負荷試験」は、低線量率長期照射の影響を検討する上で重要である。
低線量域における超高感受性も放射線感受性を修飾する要因として興味深い現象であるが、その発現の時間経過等を考えるといわゆる適応応答とは別の現象であろう。また、現在までのところ「高感受性」の指標は生存率に限られており、発がんリスクへの影響は不明である。
引用④
>○渡辺委員 そうしたら、7)Bystander効果と低線量リスクのところを読ませていただきます。
比較的短くしましたので、内容が十分盛られてないかもしれません。
放射線の遺伝的影響を評価する際に、細胞核外あるいは細胞外標的の存在に注意を払う必要性がある。1990年代半ばからアルファー線照射によって照射を受けていない隣接する細胞に突然変異を生じさせる可能性が指摘されるようになった。この効果は、“バイスタンダー効果”と総称される。最近、マイクロビーム照射技術を使ったコロンビア大学のグループは、
α粒子で細胞質のみを照射しても遺伝子突然変異が生ずることを報告した。この効果は、α線に限らずX線などでも誘導され線量効果も認められる。バイスタンダー効果で誘導される突然変異は、自然突然変異と同じように点突然変異が主流を占める。これらの事実は、放射線の遺伝的影響はDNAの損傷が直接の引き金になって生ずるとするこれまでの古典的突然変異生成機構に関する概念を覆すものである。現時点では、細胞質に生じたどのような変化が細胞核に伝えられるか明確ではない。こうした影響は、細胞質から核へと伝播されるに留まらず、隣接する細胞にも伝えられる。Mothersill は、放射線照射した細胞培養液を処理される未照射細胞の細胞死が増強されることを報告しており、細胞外標的もバイスタンダー効果の引き金になる可能性もある。バイスタンダー効果を伝播する媒体は依然明確ではないが、ある種の活性酸素ラジカルやイオンなどがギャップジャンクションを介して伝えられると予想されている。
バイスタンダー効果の存在は、放射線の真の標的は何かに疑問を投げかけるもので放射線のリスク評価のために解決すべき重要な問題である。
○丹羽主査 何かコメントございますか。
これ、拝見したあれで、「リスク評価のために解決すべき重要な問題である」の最後の下りなんですけれども、これが一般的なメカニズムであるとしたら、標的サイズがでっかくなるわけですよね。実際、リトルのグループの
α線の照射でも、例えば1%細胞に照射したんだけれども、突然変異からいったら結構たくさん出るという話で、標的サイズがでっかくなるので低線量リスクを逆に上げる側に働くという視点についてはちょっと触れておいていただいた方が、評価のために解決すべき重要な問題であるということの中身がもう少しスペシックになると思うので、そのような方がいいんじゃないかと私自身は思います。
○島田委員 さっき丹羽先生がおっしゃったんですけれども、カマタ先生たちのデータ、個体レベルのBystander効果ですよね。そういうことも含めて書いた方がいいのかなということと、あとBystanderがリスクのシチュエーションでどこで大切になるかという場合、またα線になっちゃうんですけれども、ハイラドンかなという気もしますので、そういうところでリスクとの関連で重要になってくるというふうな書き方があってもいいかなと思うんですが、渡辺先生、どうでしょうか。
○渡辺委員 わかりました。
○佐々木委員 だから、それは実験でαがやられているからラドンとかは念頭にあると思うんですけれども、要するに、荷電粒子のヒットとした場合、要するに、マイクロビームなんかを使うと何もαでもなくて、ほかのX線でも起こるわけですので、荷電粒子のヒットと考えると、何もαである必要がないのかもしれないんですよ。
それから、これはどこまであれなのかはわからないけれども、Bystander効果に適応応答があると、要するに、低線量を全照射しておくとBystander効果が抑えられるとか、それは酒井さんのところで触れるか、私はそういう報告がどこまで信用していいかもわからないけれども、そこまで書く必要はないのかもしれません。
低線量に絞るとすると、やはり非常に大きな問題であると思います。
○渡辺委員 現実、Bystanderを本当に明確に科学的に処理するためには、マイクロビームというのが非常に必要なんですけれども、世界的に使えるところが今2カ所、X線に至ってはまずゼロに近いですよね。この前、グレー行ったときも、やっとX線のマイクロビームの装置をつくったといって見せてくれましたけれども、そういう集積がないと明確なことは書けないなというのが私の一番のポイントなんですよ、いろいろなおもしろい事項はあるんだけど。で、こんなに簡単にしちゃったというのが一つなんです。
今、先生方の言われたことを入れて書き直してみますが。
○松原安全委員 ぜひ、はっきりその点お調べいただきたいんですが、この議論の初めの設定が、低線量放射線影響という言葉になっていますけれども、序文のところで、この際、低線量影響というのは、低線量リスク、すなわち発がんに絞るというふうに決めましたですよね。そして、発がんと放射線の関係について調べてくるというところできたわけなんですけれども、細胞から離れて個体レベルまでの議論に今来ているわけなんですが、そうしますと、個体レベルの発がんデータというのは非常に情報は限られていて、必ずしもすべてをカバーしていないんですね。
そうしますと、例えば、今Bystanderの話でも、突然変異という指標でもって、どのレベルで何が起こるというようなことを言ってらっしゃるんだけれども、その突然変異から後の発がんまでのプロセスについては、まだ議論されてないんじゃないかと思うんです。
それで今、世界じゅうでマイクロビームがあるところでも、突然変異まではちゃんとやったと思うんですけれども、変異細胞が発がんに至ったかというのは証明されたのかどうか、そういうようなところはないですよね。
○渡辺委員 トランスフォーメーションは。
○松原安全委員 例えば、その辺をできるだけクリアにしていただきたいと思うんです。
きょうは米沢先生のご報告を飛ばしましたんですが、米沢先生の適応応答などは、発がんを抑えるというのではなくて、やはり一般的な生体の防御機構を高めているような感じでいろいろ実験をされて、結果として生存率があれだけ低線量照射でもって、放射線による次の死亡を抑えたということで、体にとっては非常に大きなある種の生存適用性を確かめたという証拠なんですけれども、発がんということではつながらないわけですよね。ですから、この議論はどこまでが発がんで、どこから先が一般の低線量影響なのかの区別が非常にしにくくなってきましたので、その辺をどのようにさばいていただけるのかお伺いしたい。
○丹羽主査 私は十分咀嚼していないので、多分、最終的には発がんにまで持っていきたいんですけれども、Bystanderに関して言えば、セルレベルの問題でしか今のところあり得ない。ただ、現象としては一応そういうことが報告されて、もしもそれが肺の気道で起こるのであれば、肺がんのターゲットサイズはもっとでかくなるという問題提起としてこういうようなものはとらえられるであろうということは思うんですが、その突然変異からがんまでつなげということになると、これは多分全く別のチャプターを一つ立てなければならないと思うんですよね。だから、ここのところでそれを持ち出すんじゃなくて、何かもしもそれを絶対やらなきゃいかんとなったら、多分もう一つ、一こまを必ずつくって立ち上げなければならないという形で処理させていただきたいんですが。
これを議論する過程で、その問題がもっと大きい問題になってくるということになれば、この報告書で時間的な制約もございますけれども、そういうのを例えば書くなり、あるいは今回積み残して、例えば次の分科会のときにそれを取り上げていただくとか、そういうふうなことで処理したいと思うんですが。
○松原安全委員 私の希望としては、やはりBystander効果の存在というのは基本的サイズが大きなことを含めて、発がんリスクが大きくなるだろうという、そういう論理的推定にはつながります。しかし、本当にその発がんが大きくなるかという、そういう実証についてはトランスフォーメーションまであるのかもしれないけれども、はっきりした実証はまだ十分でないということ。
それから、
個々の細胞の突然変異が多くなっても、それに対して、例えば同じぐらいいろいろな防御機構とかいろいろなシグナルの活性化、それから防御機構の活性化がもし同じように誘起されてあるんであれば、先ほどの安定型突然変異で見かけ上増えないという話もあったわけですけれども、そのような個体というのはいろいろなプロセスの後の結果として発がんとか発がんじゃないという、そういう最終的な結果でもって低線量リスクというのを判定しているもんですから、そういう意味で、低線量リスクを引き上げるというようなことを書いてもいいんですけれども、それを引き上げるについては、こうこうこういうところが今後の課題であるみたいなところがある程度、そして、この分科会では、もちろん議論するのは不可能であれば、残された課題として、今後の検討すべき課題としてもぜひ、もし専門家としてコメントすることがあれば出していただいた方がよろしいんじゃないかと思います。
○丹羽主査
この議論を長いことやることは必要ないかとは思うんですが、Bystanderに関しては、現象としてまずはっきりしていて、それにインボルブしているラディカルであろうとか、そういうような役者は割とはっきりしてきているわけですよね。だから、もう一つ、生体防御機構があるというのは、多分全員アグリーするとは思うんですけれども、ここでそういう議論を取り入れるためには、その防御機構のどの防御機構が、どういう役者がどう入ってきていということをきっちり登場させない限り、かみ合った議論にならないと思うんです、報告書としては。そうすると、非常に大きな網かけとしての防御機構というものと、それで、ここで我々が議論しているような、個々の登場する役者としてのものの役割というものをある程度区別する必要があるので、多分、先生のおっしゃることは非常に重要だと思うんですが、それをこの中で同列に作業の中に入れるためには、その防御機構のおのおのの役者が今どういうのがわかってます。それがどういうふうな役目をしますというふうなことを、多分より緻密な議論が必要になるような気がしますので、ちょっとそれ、今ここでBystanderのところに持ち込むのは難しいんではないかという気はするんですが。
○松原安全委員 一般的に、私は先生のおっしゃることに同意します。といいますのは、この低線量放射線影響の分科会の検討というのが、初めのところから低線量の影響の研究と、それから放射線防護にかかわる現行の指針とのかかわりというところで問題意識を皆さんがお持ちになって、それでやってらっしゃるわけです。指針ということは、一応はICRPの発がんリスクにかかわる推定値からいろいろな基準値を議論されていると思うんです。ですから、
当然、低線量影響といったら、いろいろな影響もあるでしょうけれども、発がんをメルクマルにして議論するということでここまで来たんだと思うんです。
そうすると、発がんというのは、最後の最後のエンドポイントですから、その発がんにかかわるいろいろな知見というと、非常に膨大な量にもなるし、それを100%この段階ですべてメカニズムまではっきりしてということはできないわけだから、現状のある知見をできるだけ整理して、段階を追ってということで今まで議論してきたんです。
 【タンパク質合成系】バイスタンダー効果とプリオンの類似性【細胞質遺伝と言う概念】
【タンパク質合成系】バイスタンダー効果とプリオンの類似性【細胞質遺伝と言う概念】 






 Bystander効果から分かること【細胞には順位、そして私たちはクローン?】
Bystander効果から分かること【細胞には順位、そして私たちはクローン?】  【バイスタンダー効果】反対派のプロパガンダより、村人の密談が有意義な件。【ラジカル】
【バイスタンダー効果】反対派のプロパガンダより、村人の密談が有意義な件。【ラジカル】 


